Н. А. Дайхес1, Д. Н. Назарян1, К. С. Гилева2, М. А. Мохирев1, И. Н. Ляшев1, Г. К. Захаров1, А. В. Федосов1, М. Б. Потапов1, А. В. Батырев1 , О. В. Карнеева1
1 Национальный медицинский исследовательский центр оториноларингологии Федерального медико-биологического агентства России, Москва, Россия
2 Российский научный центр хирургии имени Б. В. Петровского, Москва, Россия
Пересадка лицевого трансплантата остается операцией выбора для пациентов собширными дефектами тканей челюстно-лицевой области. Целью работы было в эксперименте на биообъектах разработать и апробировать методику перекрестной пересадки комбинированного лицевого трансплантата, подобрать анестезиологическое пособие с целью снижения рисков периоперационных осложнений, улучшения показателей выживаемости особей за счет сокращения длительности хирургического вмешательства и разработать протокол послеоперационной терапии и реабилитации особей, оценки диагностики острой реакции отторжения и отработки иммуносупрессивной терапии. В трех сериях операций по пересадке лицевых трансплантатов на 26 минипигах были апробированы типичные комбинации компонентов и дизайны лоскута. На всех этапах эксперимента команда добилась выживания особей более 30 дней, без нарушения жизненных функций. Отработана схема иммуносупрессии. Выбранная методика позволяет проводить две пересадки за одно хирургическое вмешательство внутри одной пары.
Ключевые слова: трансплантация лица, микрохирургия, лицевой лоскут, композитный трансплантат
Финансирование: согласно гранту ФМБА на выполнение прикладной научно-исследовательской работы по теме «Исследование метаболических, морфометрических и функциональных характеристик тканей и органов после операций в области головы и шеи на основе применения физическихи лазерно-конверсионных цифровых технологий» («ЧЛХ-18»).
Вкладавторов:Н.А.Дайхес,Д.Н.Назарян—организацияработы,редактированиестатьи;К.С.Гилева,М.А.Мохирев,И.Н.Ляшев,Г.К.Захаров, А. В. Федосов, М. Б. Потапов — участие в экспериментальной части работы; А. В. Батырев — участие в организации и экспериментальной части работы, написание статьи; О. В. Карнеева — участие в организации работы.
Соблюдение этических стандартов: условия содержания животных, уход и все проводимые с ними манипуляции соответствовали стандартам работы с экспериментальными моделями.
Для корреспонденции: Алексей Владимирович Батырев
Волоколамское шоссе, д. 30/2, к. 443, г. Москва, 123182;
Статьяполучена:01.10.2020 Статьяпринятакпечати:14.11.2020 Опубликованаонлайн:29.11.2020
DOI:10.47183/mes.2020.018
ANEXPERIMENTONBIOLOGICALOBJECTS:COMPOSITEFACIALGRAFTCROSS-TRANSPLANTATION
DaikhesNA1, Nazaryan DN1, Gileva KS2, Mokhirev MA1, Lyashev IN1, Zakharov GK1, Fedosov AV1, Potapov MB1, Batyrev AV1 , Karneeva OV1
1 Federal Scientific and Clinical Center of Otorhinolaryngology under the Federal Medical-Biological Agency (FMBA) of the Russian Federation, Moscow, Russia
2 Petrovsky Russian Scientific Center for Surgery, Moscow, Russia
Facial graft transplantation remains the operation of choice for patients with extensive tissue defects in the maxillofacial region. This study aimed to set up an experiment on biological objects, develop and test a combined facial graft cross-transplantation technique, select the anesthetic aid allowing to reduce the risks of perioperative complications, improve survivability of the subjects by reducing the duration of surgical intervention, develop a postoperative therapy and rehabilitation protocol, assess detection of an acute rejection reaction and develop the immunosuppressive therapy protocol. We conducted three series of facial graft transplantation surgeries on 26 minipigs and tested the typical component combinations and flap designs. At all stages of the experiment, we managed to have the subjects surviving for over 30 days without disrupting their vital functions. The immunosuppression procedure was developed and tested. The chosen technique allows transplanting two grafts within a single surgery on one pair.
Keywords: face transplant, microsurgery, facial flap, composite flap
Funding: FMBA applied research, subject "Research of metabolic, morphometric and functional characteristics of tissues and organs after head and neck area surgery involving physical and laser-conversion digital technologies" ("ChLH-18").
Authorcontribution:Daikhes NA, Nazaryan DN — work organization, article editing; Gileva KS, Mokhirev MA, Lyashev IN, Zakharov GK, Fedosov AV, Potapov MB — participation in the experimental part of the work; Batyrev AV — participation in the organization and experimental part of the work, article authoring; Karneeva OV — participation in the organization of work.
Compliance with ethical standards: the living conditions of animals, care and all manipulations they were subjected to meet the experimental model research standards.
Correspondence should be addressed: Alexey V. Batyrev
Volokolamskoe shosse, 30/2, k. 443, Moscow, 123182;
В настоящее время основным методом реконструкции обширных дефектов головы и шеи является пластика свободными аутотрансплантатами [1–3]. Однако при утрате таких структур, как губы, веки, нос, единственным полноценным методом реабилитации таких пациентов является аллотрансплантация композитного лицевого лоскута [4–6].
На сегодняшний день в мире осуществлено 40 пересадоккомбинированноголицевоготрансплантата и, несмотря на первые удачные операции, выполненные в 2005 г. [7], операция остается уникальной и требует высокой квалификации специалистов, участвующих в подготовке, проведении оперативного вмешательства, дальнейшем наблюдении и реабилитации [8]. Большой проблемой для бригад, выполняющих данные манипуляции, остается высокая иммуногенность кожи, увеличивающая риски развития отторжения трансплантата. Единого подхода на данный момент нет и предложены различные варианты решений. Важным требованием к методикам остается гуманность экспериментов, сохранение жизни экспериментальных особей. Наиболее популярной биологической моделью для выполнения экспериментальных пересадок лицевого трансплантата до сих пор оставалась лабораторная мышь [9].
Целью работы было: 1) разработать и апробироватьв эксперименте методику перекрестной пересадки комбинированного лицевого трансплантата на минипигах;
2) разработать и апробировать послеоперационную терапию и реабилитацию особей, оценку диагностики острой реакции отторжения и формирования компетентной схемы иммуносупрессивной терапии; 3) апробировать анестезиологическое пособие с целью снижения рисков периоперационных осложнений.
МАТЕРИАЛЫ И МЕТОДЫ
Участниками эксперимента проведено три серии операций по пересадке лицевых трансплантантов на специально отобранных особях-минипигах в качестве биологических моделей.
Для проведения эксперимента были подобраны 26 близкородственных особи — братья в возрасте от 8 до 24 месяцев, весом 10–20 кг [10, 11].
Хирургическое вмешательство осуществляли параллельно на двух особях в условиях подготовленной операционной при помощи стандартного хирургического инструментария. Микроэтап осуществляли с использованием операционного микроскопа. Во время предоперационной подготовки проводили разметку комбинированного лицевого трансплантата на одной особи, далее припомощи шаблона переносили на вторую особь для достижения максимальной прецизионности. При заборе трансплантатов производили острую мобилизацию мягкотканных компонентов лоскутов, с сохранением жизненно важных структур, оставляли сохранными сосудистые пучки до уровня отхождения от наружных сонных артерий и впадения в яремные вены,выделяливетвилицевогонервадляпоследующей нейрорафии. Костные части трансплантатов атравматично мобилизовали при помощи пьезохирургического аппарата, после трансплантации фиксировали минипластинами и минивинтами Конмет. В послеоперационном периоде динамически на 7-е, 14-е, 21-е сутки проводили забор биоптатов для верификации протекающих репаративных процессов. При появлении первых признаков реакции отторжения проводили забор биоптата вне стандартных сроков. На всех этапах эксперимента вели фото- и видеофиксацию (рис. 1, 2). Были рассмотрены различные комбинации лоскутов с целью отработки наиболее распространенных вариантов трансплантатов (табл. 1).

Рис. 1. Экспериментальные особи в ближайший послеоперационный период

Рис. 2. Минипиги на 14-е сутки после проведенной кросс- трансплантации
Таблица 1. Использование моделей лоскутов на различных этапах эксперимента
|
Число особей |
Возраст (месяцы) |
Дизайн трансплантата |
|
1-йэтап |
||
|
4 |
24 |
Лицевойкожно-мышечный лоскутщечной, околоушнойобластей (рис.3, 4) |
|
4 |
24 |
Комбинированныйкожно-костно-мышечныйлоскутщечной,околоушнойобластейинижнейчелюсти(рис.5,6) |
|
2 |
24 |
Комбинированныйкожно-костно-мышечныйлоскутпараорбитальной,щечной,околоушнойобластейиверхнейчелюсти |
|
2-йэтап |
||
|
2 |
24 |
Лицевой кожно-мышечный лоскут щечной,околоушной, нижней частипараорбитальной областей (рис. 7,8) |
|
2 |
8 |
Лицевой кожно-мышечный лоскут щечной,околоушной, нижней частипараорбитальной областей (рис. 9,10) |
|
2 |
24 |
Лицевойкожно-мышечныйлоскутоколоушнойобластисушнойраковинойищечнойобласти |
|
2 |
8 |
Лицевойкожно-мышечныйлоскутоколоушнойобластисушнойраковинойищечнойобласти |
|
3-йэтап |
||
|
4 |
8 |
Лицевой кожно-мышечный лоскут щечной и околоушной областей с наложением нейроанастомозов в областиветвей лицевого нерва |
|
4 |
8 |
Лицевой кожно-мышечный лоскут околоушной области с включением наружного отдела ушной раковины,щечной области с наложением нейроанастомозов в области ветвей лицевого нерва |
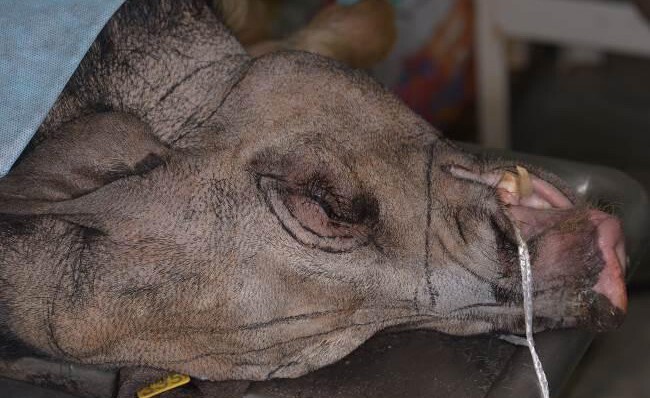
Рис.3.Лицевой кожно-мышечный лоскут щечной, околоушной областей (перваяособь)
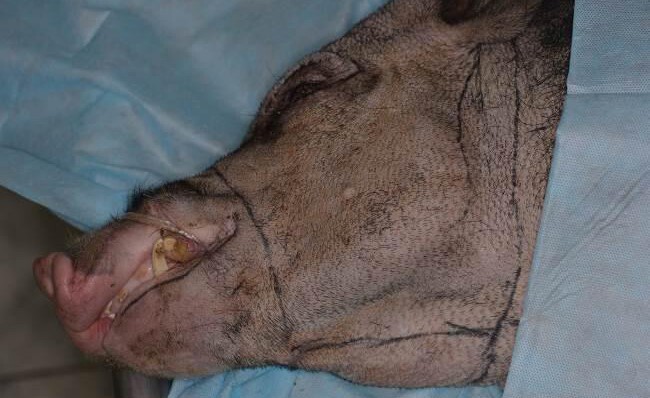
Рис.4.Лицевой кожно-мышечный лоскут щечной, околоушной областей (втораяособь)
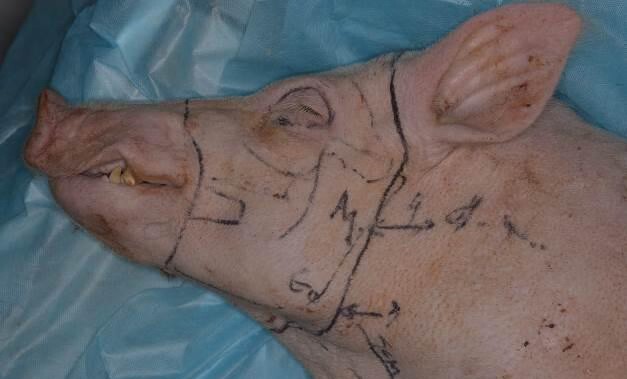
Рис.5.Комбинированныйкожно-костно-мышечныйлоскутщечной,околоушной областей и нижней челюсти (первая особь)
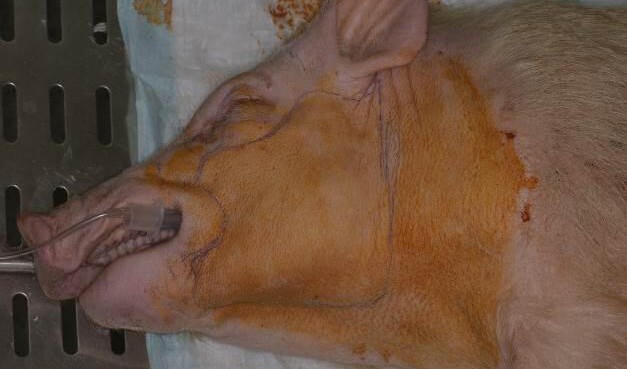
Рис.6.Комбинированныйкожно-костно-мышечныйлоскутщечной, околоушной областей и нижней челюсти (вторая особь)
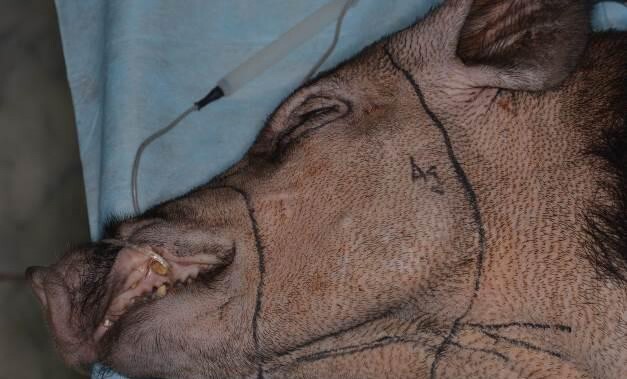
Рис.7.Лицевойкожно-мышечныйлоскутщечной,околоушной,нижней части параорбитальной областей (первая особь)
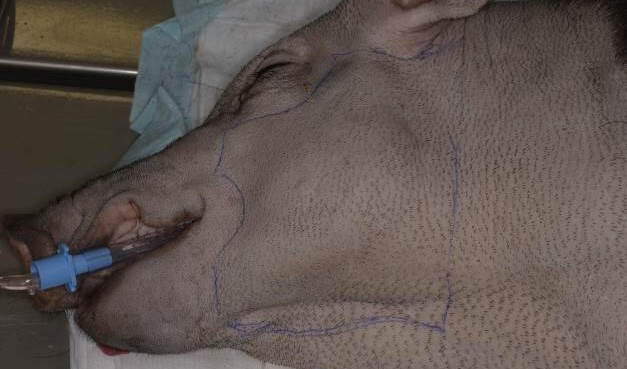
Рис.8.Лицевойкожно-мышечныйлоскутщечной,околоушной,нижней части параорбитальной областей (вторая особь)
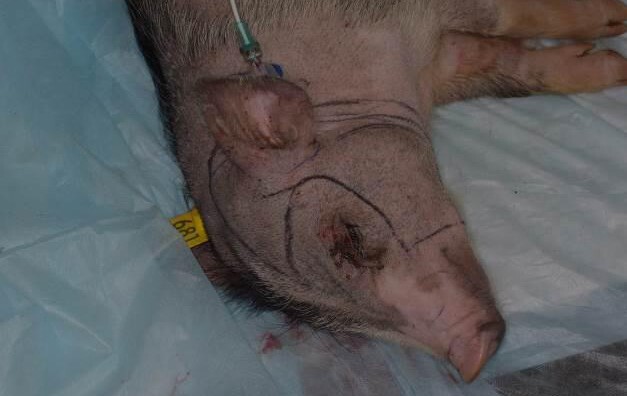
Рис. 9. Лицевой кожно-мышечный лоскут околоушной области с ушной раковиной и щечной области (первая особь)
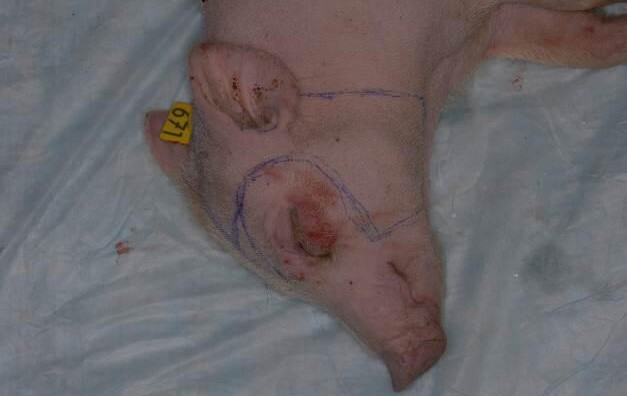
Рис. 10. Лицевой кожно-мышечный лоскут околоушной области с ушной раковиной и щечной области (вторая особь)
Входепервогоэтапанапятипарахминипигов(пары— братья, возраст — 24 месяца, вес — 16–20 кг) выполнили экспериментальные перекрестные пересадки лицевых трансплантатов, в ходе которых были апробированыи отработаны основные методики и дизайны лоскутов с отработкой ключевых этапов (рис. 11–13):
лицевой кожно-мышечный лоскут щечной, околоушной областей;комбинированный кожно-костно-мышечный лоскут щечной, околоушной областей и нижней челюсти;комбинированный кожно-костно-мышечный лоскут параорбитальной, щечной, околоушной областей и верхней челюсти.
Оперативные вмешательства проводили в условиях внутривенногонаркоза(рометар0,15мг/кг+золетил-100 2 мг/кг) без анестезиологического сопровождения. Среднее время оперативного вмешательства составило 14 ч.
В послеоперационном периоде животные получали антибактериальный препарат (байтрил — 14 суток) и иммуносупрессивную терапию (преднизолон 120 мг в/м 1раз/сут.втечениевсегопериоданаблюдения).
В послеоперационном периоде у двух особей из разных пар отмечено развитие отека на 5-е сутки после оперативного вмешательства, им проводили пульс- терапиюиувеличилиплановуюдозировкупреднизолона до 240 мг. Спустя 5 дней произошел тромбоз анастомозоввследствиеразвитиясосудистойреакциина гиперергический ответ организма реципиента.
Выполнение 2-го этапа
В ходе второго этапа производили перекрестную пересадку лицевого трансплантата на четырех парах особей (две пары — братья, возраст — 24 месяца, вес — 20 кг; две пары — братья, возраст — 8 месяцев, вес — 8 кг).
Вданномэкспериментеапробироваликросс-трансплантацию:
лицевого кожно-мышечного лоскута щечной, околоушной, нижней части параорбитальной областей;лицевогокожно-мышечноголоскутаоколоушной области с ушной раковиной и щечной области.
Оперативные вмешательства проводили с анестезиологическим пособием, внутривенной седацией (рометар 0,15 мг/кг, золетил-100 2 мг/кг, пропофол 4 мг/кг, ксила 0,2 мл/кг) под контролем врачей-анестезиологов. Среднее время оперативного вмешательства составило 10 ч. В послеоперационном периоде экспериментальные особи получали антибактериальную (байтрил — 3 мл 1 раз/ сутки в/м) и иммунотерапию (дексаметазон 16 мг 1 раз/
сутки в/м) в течение всего времени наблюдения.
Так же как и на 1-м этапе эксперимента, было отмечено отсроченное развитие реакции отторжения. Клинические проявления купировали с помощью пульс-терапии гормонального препарата солумедрол 360 мг в/м.
На 21-е сутки после хирургического вмешательства был произведен забор гистологического материала (место сращения пересаженного лоскута и тканей реципиентной особи) для гистологического контроля.
Выполнение 3-го этапа
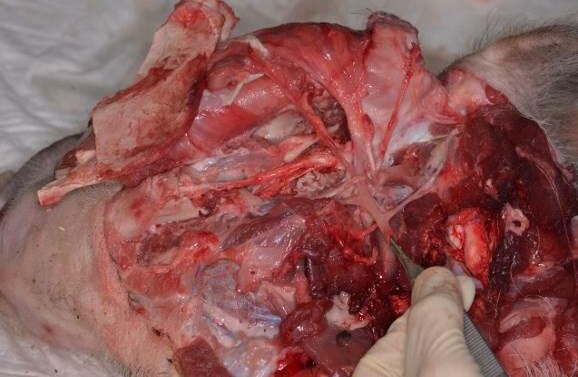
Рис. 11. Интраоперационное фото после диссекции комбинированного кожно-костно-мышечного лоскута щечной области
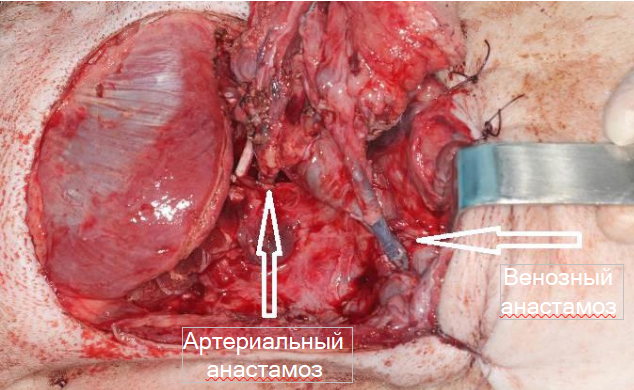
Рис. 12. Интраоперационное фото после диссекции комбинированного кожно-костно-мышечного лоскута щечной области и нижней челюсти
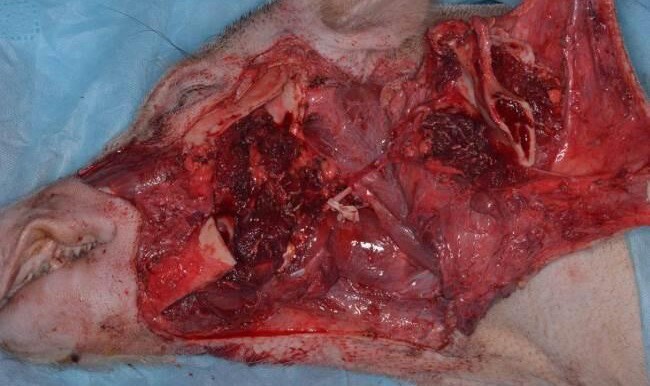
Рис. 13. Интраоперационная фотография, сделанная после наложения сосудистыханастомозов
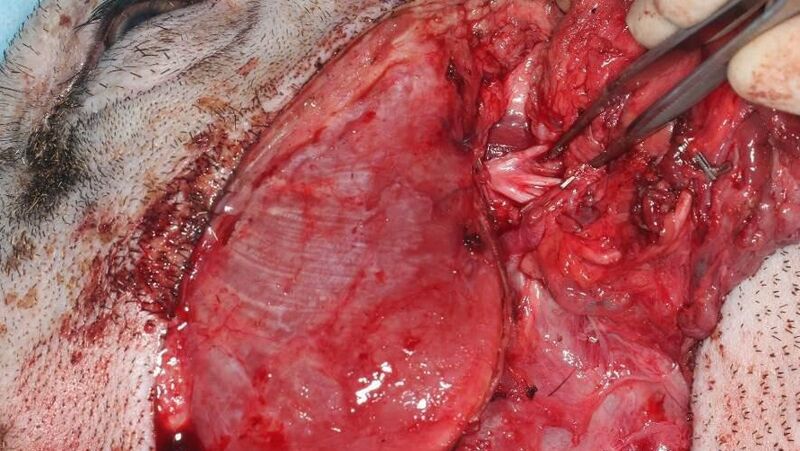
Рис. 14. Интраоперационная фотография, сделанная после выделенного ствола и ветвей лицевого нерва
Таблица 2. Время наблюдения на каждом этапе эксперимента
|
Число особей |
Возраст(месяцы) |
Длительность наблюдения за лоскутом |
|
1-йэтап |
||
|
Двепары(реципиент–донор) |
24 |
36дней |
|
2-йэтап |
||
|
Двеособи из разных пар |
8 |
30дней(сгистологическимподтверждениемна 21-е сутки заживления первичнымнатяжением) |
|
3-йэтап |
||
|
Двеособи из разных пар (сприменениемпрепарататакролимус) |
8 |
30дней(сгистологическимподтверждениемна 14-е сутки заживления первичнымнатяжением) |
Таблица 3. Выживаемость особей после проведенного оперативного вмешательства
|
Число особей |
Длительность |
|
1-йэтап |
|
|
8из 10 (80%) |
Более30 дней |
|
2-йэтап |
|
|
7из 8 (87,5%) |
Более30 дней |
|
3-йэтап |
|
|
7из 8 (87,5%) |
Более30 дней |
особей (четыре пары — братья, возраст — 8 месяцев, вес — 10 кг). В результате анализа проведенной работы была скорректирована периоперационная терапия, изменен протокол анестезии. Интра- и послеоперационно проводили иммуносупрессивную терапию [12].
Для профилактики немедленной потери трансплантатов по иммунологическим причинам накануне операции проводили определение совместимости групп крови и микролимфоцитотоксический тест, при этом учитывали, что каждое животное одновременно являлось и донором, и реципиентом. Индивидуальную совместимость крови проверяли, ставя пробу на плоскости при комнатной температуре.
В результате серии иммунологических тестов было сформировано четыре пары животных, которым совокупно выполнили восемь трансплантаций — в каждом случае результаты пробы на индивидуальную совместимость и микролимфоцитотоксический тест были отрицательными.
В данном эксперименте была продолжена отработка моделей комбинированных лоскутов:
лицевого кожно-мышечного лоскута щечной и околоушной областей с наложением нейроанастомозов в области ветвей лицевого нерва;лицевого кожно-мышечного лоскута околоушной области с включением наружного отдела ушной раковины, щечной области с наложением нейроанастомозов в области ветвей лицевого нерва (рис. 14).
Оперативное вмешательство проводили с анестезиологическим пособием под внутривенной седацией (золетил-100 2 мг/кг, пропофол — 4 мг/кг, ксила — 0,2 мл/кг). Среднее время оперативного вмешательства составило 8 ч. В медикаментозную терапию в ходе эксперимента с учетом дополнительных консультаций с трансплантологами и анестезиологами были внесены следующие корректировки.
Предоперационный период:
за 8ч—низкомолекулярные гепарины (клексан) п/к; антибактериальная терапия — за 30 мин до разреза интерспектин 1 мл в/в.
Интраоперационно две пары особей получали: в/в «Прогаф» (0,15 мг/кг);
гепарин перед запуском кровотока.
В послеоперационном периоде экспериментальным особям назначены: антибактериальные препараты (интерспектин 1 мл на 10 кг в/м 1 раз/сутки) в течение 14 дней для профилактики вторичных бактериальных осложнений; иммуносупрессивная терапия (Солумедрол 160мгв/м) в течение всего периода наблюдения.
В послеоперационном периоде не было отмечено выраженных явлений отторжения лоскутов, сохраняющиеся отеки были обусловлены объемом вмешательства и гиперсекрецией слюнной железы.
РЕЗУЛЬТАТЫ ИССЛЕДОВАНИЯ
На всех этапах эксперимента достигнуто выживание особей в долгосрочном периоде, что свидетельствует о гуманном использовании животных. Жизненные функции особей в послеоперационном периоде остались без изменений (табл. 2). Достигнуто улучшение выживаемости особей после оперативного вмешательства (табл. 3).
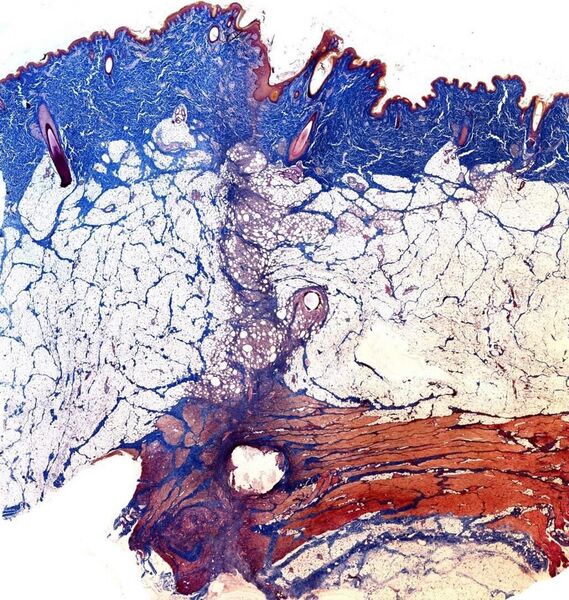
Рис.15.Местосращениялоскутастканямиреципиентанасканированном изображении гистологического препарата
Таблица 4. Результаты выживания лоскутов в зависимости от применения различных видов антибактериальной и иммуносупрессивной терапии
|
Иммунотерапия |
Результат |
|
1-йэтап |
|
|
Антибактериальная (цефтриаксон 1 раз/сутки в/м) +иммуносупрессивнаятерапия (преднизолон120мг,приразвитииотторжения пульс-терапия 240 мг) |
Два (из 10) лоскута из разных пар — выживание без признаков острогоотторжениядо36дней,развитиеотсроченногоострогоотторжения спопыткой купирования пульс-терапией |
|
2-йэтап |
|
|
Антибактериальная (энрофлоксацин — 1 раз/сутки в/м) и иммунотерапия(дексаметазон 16 мг 1 раз/сутки в/м, при развитии реакции отторжения пульс-терапия дексаметазон 32 мг 1 раз/сутки) |
Два(из8)лоскутаизразныхпар—приживлениена21-есутки, с купированным острым кризом отторжения в послеоперационномпериоде |
|
3-йэтап |
|
|
Антибактериальная(линкомицин+спектиномицин1раз/суткив/м)ииммунотерапия(такролимус—интраоперационнов/в,метилпреднизолонв/м) |
Два (из 8) лоскута из разных пар — приживление на 14-е суткибез явлений отторжения |
При гистологическом исследовании (рис. 15) границ реципиент–донор получены результаты заживления первичнымнатяжением,исключаяостроеотторжениепо Banff-классификации [13, 14].
На рис. 15 представлены кожа и подкожная клетчатка, состоящие из двух фрагментов, разделенных раневым пространством.
Первый фрагмент (реципиент) — кожный лоскут с платизмой. Кожа представлена обычными слоями с признаками ороговения, производными кожи (волосяными фолликулами, сальными железами). Жировая клетчатка включает сосуды различного калибра. Платизма обычного строения состоит из продольных и поперечных мышечных волокон. В глубоком слое — железистые структуры.
Второйфрагмент—кожныйлоскутсплатизмой.Кожа представлена обычными слоями с признаками ороговения, производными кожи (волосяными фолликулами, сальными железами). Жировая клетчатка включает сосуды различного калибра. В платизму обычного строения состоящую из продольных и поперечных мышечных волокон, проникают узкие тяжи грануляционной ткани. Сосуды содержат форменные элементы.
Раневое пространство представлено узкой щелью, заполненной грануляционной тканью с низкой клеточностью. Основу грануляционной ткани составляют мелкие капилляры и прослойки соединительной ткани с тонкими фибриллами. Грануляционная ткань практически без инфильтрации полиморфноядерными лейкоцитами (нейтрофилами), лимфоцитами. Они обнаруживаются лишь в поверхностном слое под некротизированным участком эпидермиса. По ходу раневой щели только со стороны первого фрагмента заметна инфильтрация многоядерными клетками.
В табл. 4 представлены результаты приживления лоскутов в зависимости от схем терапии в пери- и послеоперационном периодах. Следует отметить более эффективный ответ при купировании реакций острого отторжения.
ОБСУЖДЕНИЕРЕЗУЛЬТАТОВ
В послеоперационном периоде, несмотря на гистологическую верификацию заживления трансплантатов, необходимо активное динамическое наблюдение с
минимальной задержкой коррекции иммуносупрессивной терапии при появлении признаков развития острой реакции отторжения тканей.
После анализа результатов эксперимента в связи с развитием кризов острого отторжения трансплантата, нами сделан вывод о необходимости продолжения разработки и апробации схемы иммуносупрессии, что согласуется с результатами других исследователей [15]. Другой группой авторов выявлена роль особенности композитного трансплантата в развитии реакции отторжения в одном из его компонентов [16], ведущей к потере кожной части лоскута, но с сохранностью мышечного компонента.
Такимобразом,поднимаетсявопросонеобходимости подбора объективных методов диагностики состояния всех компонентов лоскута и важности учета особенностей композитных трансплантатов, по сравнению с трансплантацией единых органов.
ВЫВОДЫ
Апробированнаявэкспериментеметодикаперекрестной пересадки комбинированного лицевого трансплантата позволяет отработать навыки всем членам бригады (хирургам, анестезиологам, трансплантологам, иммунологам), участвующим в подготовке, проведениии послеоперационной реабилитации пациентов с предстоящейоперациейпотрансплантациилица. При проведении манипуляций с расширенным анестезиологическим пособием отмечено сокращение операционного времени и улучшение показателя выживаемости особей после операции.
Используемая на данном этапе эксперимента иммуносупрессивная терапия требует дальнейшей коррекции и апробации для снижения риска развития эпизодов острого или хронического отторжения.
Акцент на уникальных особенностях композитных трансплантатов может позволить использовать дополнительное,болееспецифичноелечение,чтоможет кратно увеличить длительность жизни пациентов с данным видом трансплантатов. С учетом вышеописанных факторов стоит рассмотреть возможность применения препарата алемтузумаб в периоперационном периоде дополнительно к применяемой схеме при проведении трансплантаций.
Литература
1. Fu-Chan Wei, Mardini S. Flaps and Reconstructive Surgery. Elsevier, 2016; 872 p.
2. Пейпл А. Д., редактор. Пластическая и реконструктивная хирургиялица.М.:Бином.Лабораториязнаний,2007;952с.
3. Неробеев А. И., Плотников Н. А. Восстановительная хирургия мягких тканей челюстно-лицевой области. М.: Медицина; 288 с.
4. Sosin M, Ceradini DJ, Levine JP, Hazen A, Staffenberg DA, SaadehPB,etal.TotalFace,Eyelids,Ears,Scalp,andSkeletal SubunitTransplant.PlasticandReconstructiveSurgery.2016; 138 (1): 205–19.
5. Pomahac B, Diaz-Siso JR, Bueno EM. Evolution of indications for facial transplantation. Journal of Plastic, Reconstructive Aesthetic Surgery. 2011; 64 (11): 1410–6.
6. Wo L, Bueno E, Pomahac B. Facial transplantation. Current OpinioninOrganTransplantation.2015;1.
7. Iske J, Nian Y, Maenosono R. Maurer M, Sauer IM, Tullius SG. Composite tissue allotransplantation: opportunities and Challenges. Cellular Molecular Immunology. 2019; 16: 343–9
8. Siemionow M. The Know-How of Face Transplantation. L.: Springer-Verlag, 2011; 494 р.
9. SiemionowM.PlasticandReconstructiveSurgeryExperimental ModelsandResearchDesigns.L.:Springer-Verlag,2015;661р.
10. Каркищенко Н. Н., Грачев С. В. Руководство по лабораторным животным и альтернативным моделям в биомедицинских исследованиях. М.: Профиль-2C, 2010; 344 с.
11. Руководство по работе с лабораторными животными для сотрудниковГБОУВПОРНИМУим.Н.И.ПироговаМинздрава России, занятых проведением доклинических испытаний. М., 2015; 42 с.
12. Rifkin WJ, David JA, Plana NM, Kantar RS, Diaz-Siso JR, Gelb BE, et al. Achievements and Challenges in Facial Transplantation. Annals of Surgery. 2018; 268 (2): 260–70.
13. SolezK,RacusenLC.TheBanffclassificationrevisited.Kidney International. 2013; 83 (2): 201–06.
14. Schneider M, Cardones ARG, Selim MA, Cendales LC. Vascularized composite allotransplantation: a closer look at the banff working classification. Transplant International. 2016; 29 (6): 663–71.
15. Kueckelhaus M, Fischer S, Seyda M, Bueno EM, Aycart MA, AlhefziM,etal.Vascularizedcompositeallotransplantation:current standards and novel approaches to prevent acute rejection and chronic allograft deterioration. Transplant International. 2015; 29
(6):655–62.
16. Sinha I, Pomahac B. Split rejection in vascularized composite allotransplantation.Eplasty.2013;13:e53.
References
1. Fu-Chan Wei, Mardini S. Flaps and Reconstructive Surgery. Elsevier, 2016; 872 p.
2. Pejpl AD, redaktor. Plasticheskaja i rekonstruktivnaja hirurgija lica. M.:Binom.Laboratorijaznanij,2007;952s.Russian.
3. Nerobeev AI, Plotnikov NA. Vosstanovitel'naja hirurgija mjagkih tkanej cheljustno-licevoj oblasti. M.: Medicina; 288 s. Russian.
4. Sosin M, Ceradini DJ, Levine JP, Hazen A, Staffenberg DA, Saadeh PB, et al. Total Face, Eyelids, Ears, Scalp, and Skeletal Subunit Transplant. Plastic and Reconstructive Surgery. 2016; 138 (1): 205–19.
5. Pomahac B, Diaz-Siso JR, Bueno EM. Evolution of indications for facial transplantation. Journal of Plastic, Reconstructive Aesthetic Surgery. 2011; 64 (11): 1410–6.
6. Wo L, Bueno E, Pomahac B. Facial transplantation. Current OpinioninOrganTransplantation.2015;1.
7. Iske J, Nian Y, Maenosono R. Maurer M, Sauer IM, Tullius SG. Composite tissue allotransplantation: opportunities and Challenges. Cellular Molecular Immunology. 2019; 16: 343–9
8. Siemionow M. The Know-How of Face Transplantation. L.: Springer-Verlag, 2011; 494 р.
9. SiemionowM.PlasticandReconstructiveSurgeryExperimental ModelsandResearchDesigns.L.:Springer-Verlag,2015;661р.
10. Karkishhenko NN, Grachev SV. Rukovodstvo po laboratornym zhivotnym i al'ternativnym modeljam v biomedicinskih issledovanijah. M.: Profil'-2C, 2010; 344 s. Russian.
11. Rukovodstvo po rabote s laboratornymi zhivotnymi dlja sotrudnikov GBOU VPO RNIMU im. N.I.Pirogova Minzdrava Rossii, zanjatyh provedeniem doklinicheskih ispytanij. M., 2015; 42 s. Russian.
12. Rifkin WJ, David JA, Plana NM, Kantar RS, Diaz-Siso JR, Gelb BE, et al. Achievements and Challenges in Facial Transplantation. Annals of Surgery. 2018; 268 (2): 260–70.
13. SolezK,RacusenLC.TheBanffclassificationrevisited.Kidney International. 2013; 83 (2): 201–06.
14. Schneider M, Cardones ARG, Selim MA, Cendales LC. Vascularized composite allotransplantation: a closer look at the banff working classification. Transplant International. 2016; 29 (6): 663–71.
15. Kueckelhaus M, Fischer S, Seyda M, Bueno EM, Aycart MA, AlhefziM,etal.Vascularizedcompositeallotransplantation:current standards and novel approaches to prevent acute rejection and chronic allograft deterioration. Transplant International. 2015; 29
(6):655–62.
16. Sinha I, Pomahac B. Split rejection in vascularized composite allotransplantation.Eplasty.2013;13:e53.
